La rinascita dell’atomismo in Europa: la scoperta dell’elettrone
In Europa l’atomismo vide la sua rinascita tra il 1600 e il 1700 con lo svilupparsi del metodo scientifico: scienziati e filosofi come Cartesio, Hobbes, Bacone, Giordano Bruno accettarono l’idea atomista. Anche Galilei formulò una sua teoria corpuscolare e con essa riuscì a giustificare il concetto di inerzia. Ma la teoria Cartesiana, il corpuscolarismo, risultò comunque la più completa.
Un altro personaggio di rilievo che fece la sua comparsa nella seconda metà del Seicento fu Boyle, il quale, interiorizzando il metodo empirico di Bacone, ricondusse le proprietà degli oggetti macroscopici alle caratteristiche degli atomi invisibili, chiamati minima naturalia.
Iniziò, dunque, a svilupparsi in Europa quella che venne chiamata “filosofia meccanica”.
Nel 1808, grazie allo sviluppo della tecnologia, Johann Dalton riuscì ad acquisire prove  empiriche sulla composizione della materia. Egli notò che le sostanze potevano essere scomposte in elementi più semplici e questi si presentavano sempre nelle stesse proporzioni di peso. Ciò gli suggerì che gli atomi di un dato elemento potevano combinarsi solo con un numero limitato di atomi di altri elementi per formare le sostanze. Anche Avogadro e Mendeleev trassero importanti conclusioni dallo studio del peso degli elementi: Avogadro scoprì che alla stessa temperatura e pressione, uguali volumi di gas avevano lo stesso numero di molecole e quindi, pesando i volumi dei gas era possibile determinare i rapporti delle masse atomiche.
empiriche sulla composizione della materia. Egli notò che le sostanze potevano essere scomposte in elementi più semplici e questi si presentavano sempre nelle stesse proporzioni di peso. Ciò gli suggerì che gli atomi di un dato elemento potevano combinarsi solo con un numero limitato di atomi di altri elementi per formare le sostanze. Anche Avogadro e Mendeleev trassero importanti conclusioni dallo studio del peso degli elementi: Avogadro scoprì che alla stessa temperatura e pressione, uguali volumi di gas avevano lo stesso numero di molecole e quindi, pesando i volumi dei gas era possibile determinare i rapporti delle masse atomiche.
Lavoisier, applicando il metodo scientifico alla chimica, giunse alla legge di conservazione della massa contraddicendo le teorie alchemiche medioevali secondo cui un elemento poteva essere trasmutato in un altro.
 A Mendeleev si deve la tavola periodica degli elementi, una tabella in cui gli atomi risultano classificati in base alle loro proprietà. Al suo tempo ancora non si sapeva bene cosa fossero gli atomi, ma non sarebbe passato molto affinché venissero chiariti dei punti in questo senso.
A Mendeleev si deve la tavola periodica degli elementi, una tabella in cui gli atomi risultano classificati in base alle loro proprietà. Al suo tempo ancora non si sapeva bene cosa fossero gli atomi, ma non sarebbe passato molto affinché venissero chiariti dei punti in questo senso.
Nel corso dell’Ottocento Maxwell unificò le forze magnetiche a quelle elettriche, vennero scoperti i raggi X e, più o meno nello stesso periodo, i coniugi Curie scoprirono gli elementi radioattivi. Ad aprire la finestra sulla struttura atomica fu, però, la scoperta dell’elettrone nel 1896 a opera del fisico britannico Joseph Thomson.
Thomson si accorse che se si prendeva un tubo, contenente un gas e in cui si faceva passare corrente elettrica da un catodo a un anodo, e vi si applicava un campo magnetico, i raggi catodici venivano deviati. Dall’entità di questa deviazione era  possibile misurare il rapporto della carica elettrica rispetto alla massa dei raggi catodici: questi ultimi erano in realtà delle particelle cariche negativamente (elettroni) così piccole che dovevano essere contenute in tutti gli atomi. Il nome “elettrone”, già coniato nel 1874 dal fisico irlandese George Stoney, fu proposto per identificare tali particelle dal fisico irlandese George F. Flitzgerard e da allora venne universalmente accettato.
possibile misurare il rapporto della carica elettrica rispetto alla massa dei raggi catodici: questi ultimi erano in realtà delle particelle cariche negativamente (elettroni) così piccole che dovevano essere contenute in tutti gli atomi. Il nome “elettrone”, già coniato nel 1874 dal fisico irlandese George Stoney, fu proposto per identificare tali particelle dal fisico irlandese George F. Flitzgerard e da allora venne universalmente accettato.
Essendo gli atomi elettricamente neutri, l’esistenza di particelle negative comportava l’esistenza di particelle positive tali da bilanciarle. 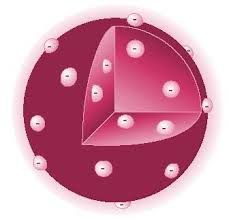 Il fisico britannico elaborò allora un modello (detto a panettone) secondo cui in una sfera carica positivamente, grandequanto l’atomo, erano sparsi in modo omogeneo gli elettroni. L’esperimento di Thomson permise di capire che il numero atomico della tavola periodica rappresentava il numero degli elettroni che componevano l’atomo, la cui posizione era definita dalla legge di repulsione elettrostatica scoperta da Coulomb un secolo prima.
Il fisico britannico elaborò allora un modello (detto a panettone) secondo cui in una sfera carica positivamente, grandequanto l’atomo, erano sparsi in modo omogeneo gli elettroni. L’esperimento di Thomson permise di capire che il numero atomico della tavola periodica rappresentava il numero degli elettroni che componevano l’atomo, la cui posizione era definita dalla legge di repulsione elettrostatica scoperta da Coulomb un secolo prima.
La scoperta dell’elettrone valse a Thomson il nobel che gli fu consegnato nel 1906.


